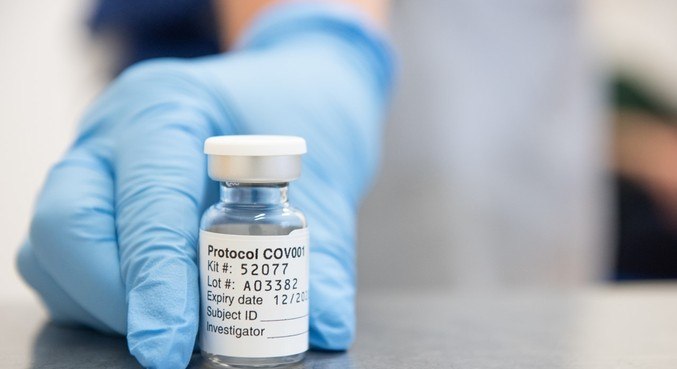
Anvisa autoriza importação de vacinas pela Fiocruz
r7 -02/01/2021 23:42
A Anvisa (Agência Nacional de Vigilância Sanitária),
anunciou neste sábado (2), que liberou a importação excepcional de 2 milhões de
doses da vacina da Oxford/AstraZeneca contra o novo coronavírus pela Fiocruz. A
decisão foi assinada na última quinta, 31 de dezembro, segundo a nota, mesmo
dia em que a Fiocruz entrou com o pedido para importar o imunizante.
A importação é considerada excepcional porque o uso do
medicamento ainda não foi autorizado formalmente pela agência, mas será trazido
ao país para que a vacinação possa ser iniciada imediatamente após o uso ser
liberado, possivelmente ainda neste mês. A Fiocruz disse que fará o pedido de utilização até o próximo dia 6,
"De acordo com o pedido da Fiocruz, a importação
excepcional é uma preparação para antecipar a disponibilização de vacinas a
partir do momento em que o seu produto estiver aprovado pela Anvisa", diz
o comunicado da agência.
Como se trata de uma autorização emergencial, a Anvisa
estabeleceu algumas regras. A mais importante é que todas as doses serão
armazenadas pela Fiocruz, que tem parceria com a Oxford e a AstraZeneca, até
que o uso seja liberado. Corrida para a vacinação
A Anvisa estima que avaliará pedidos de uso emergencial de
vacinas em no máximo dez dias. A diretora responsável pela área de vacinas,
Meiruze Fritas, disse, em entrevista ao Estadão, que o aval pode ser dado até
mais cedo, pois serão considerados os dados já apresentados pelas
farmacêuticas. Com esta permissão, é possível começar a vacinação em grupos
restritos pelo SUS (Sistema Único de Saúde), como de profissionais de saúde ou
idosos.
A ideia é distribuir 210,4 milhões de doses em 2021, que serviriam para
imunizar mais de 105 milhões de pessoas. O governo investiu cerca de R$ 2
bilhões para a compra de doses e transferência de tecnologia para a Fiocruz. No
PNI (Plano Nacional de Imunização), o governo prevê aplicar doses desta vacina
em cerca de 50 milhões de brasileiros de grupos prioritários ainda no primeiro
semestre.
"Essas vacinas serão fornecidas pelo Serum Institute of
India, parceiro tecnológico da Fiocruz, fornecedor do PNI e ator central na
produção e distribuição em escala global dessa vacina, inclusive por intermédio
da iniciativa COVAX.
No entanto, para levarmos a cabo essa operação, faz-se
necessária a autorização prévia da Anvisa para importação dessa vacina em
caráter de excepcionalidade", informa a Fiocruz à Agência Estado. Ao pedir
a liberação da importação, o laboratório coloca como justificativa a
"situação de emergência sanitária que requer o início da vacinação no
menor prazo possível."
Responsável por coordenar o estudo clínico da vacina no
Brasil, a médica Lily Yin Weckx disse ao Estadão que a primeira dose da vacina
já mostra eficácia de cerca de 70% contra a doença, mas em intervalo curto.
"A gente ainda pode ficar com a média de eficácia de
70%. O estudo continua, teremos um ano de segmento para ver a persistência da
proteção, dos anticorpos, de segurança, etc. O que é importante é que temos uma
vacina segura, eficaz e que pode fazer a diferença na pandemia.
Esses números de 60%, 70%, 80% são de proteção contra a
doença covid. Mas se considerarmos doenças graves e hospitalização, a vacina
foi capaz de evitar quase 100%. Entre as pessoas que foram vacinadas, nenhuma
delas teve uma doença grave nem ficou hospitalizada por covid. Todas as
hospitalizações ocorreram no grupo controle", disse a médica.